08 de abril de 2026 · Diego Mendes de Souza
App open source na triagem de metanol em bebidas e combustíveis: entenda a metodologia do AlcoLab
AlcoLab: ferramenta gratuita e open source para triagem de metanol em bebidas e em combustíveis usando seringa, balança e smartphone. Base científica, viscosidade e densidade.

O delegado-geral da Polícia de São Paulo, Artur Dian, disse no final de outubro de 2025:
Todas as bebidas adulteradas com metanol no estado saíam de uma fábrica clandestina gerenciada por uma família em São Bernardo do Campo. O etanol adulterado com metanol era adquirido em dois postos de combustíveis da região pertencentes à facção criminosa PCC [1].
São Paulo foi disparado o estado mais afetado pelas intoxicações por metanol. Pelo balanço final consolidado pelo Ministério da Saúde, das 890 notificações registradas entre 26 de setembro e 5 de dezembro, São Paulo concentrou 578 delas e 50 dos 73 casos confirmados nacionalmente, além de 10 dos 22 óbitos confirmados [2].
Embora em muitos casos não tenha sido determinada a rota do metanol presente nas garrafas de destilados, o maior caso de adulteração elucidado em São Paulo sugere interconexão entre adulteração de combustível, adulteração de bebidas e casos de intoxicação por metanol.

Da matriz energética brasileira à adulteração do etanol combustível com metanol
- Etanol hidratado combustível (EHC) um dos pilares da matriz energética brasileira, com produção anual superior a 30 bilhões de litros para mais de 40 milhões de veículos [3];
- Comercializado em mais de 42 mil postos, com qualidade monitorada pela Agência Nacional do Petróleo, Gás Natural e Biocombustíveis (ANP), por meio do Programa de Monitoramento da Qualidade dos Combustíveis (PMQC) e de fiscalizações diretas [4];
- Historicamente, as fraudes mais comuns envolviam a adição excessiva de água ao EHC e a mistura de solventes mais baratos à gasolina;
- A adulteração de combustíveis com metanol é motivada por um diferencial de preço significativo. Em 2024–2025 o preço médio do metanol industrial importado ficou bem abaixo do custo do etanol hidratado das usinas [5,6];
- Essa diferença de ~50% gera margens ilícitas expressivas, amplificadas pela sonegação fiscal que frequentemente acompanha o esquema [5,6];
- Operação Carbono Oculto da Polícia Federal em conjunto com o Ministério Público, agosto de 2025, revelou esquema bilionário envolvendo importação irregular de metanol pelo Porto de Paranaguá e distribuição a postos de combustíveis controlados por organização criminosa [7,8];
- Combustível adulterado continha até 90% de metanol, 180 vezes mais que o limite 0,5% v/v permitido pela ANP [8].
Intoxicação por metanol pela adulteração de bebidas com metanol
O consumidor não distingue uma bebida adulterada pelo gosto, pelo cheiro ou pela aparência — e essa similaridade é a raiz do problema de saúde pública. O diferencial, no entanto, é toxicológico: metabolizado pela álcool desidrogenase a formaldeído e depois a ácido fórmico, o metanol causa acidose metabólica e lesão irreversível do nervo óptico e dos núcleos putaminais [9–11].
- Dose potencialmente letal em adulto: ~30 mL de metanol puro; ~10 mL já podem causar cegueira permanente [12,13].
- Concentrações sanguíneas letais: 118–257 mg/dL; mortalidade de até 50 % em hospitais com diagnóstico limitado [14,15].
- Latência clínica típica: 12–24 h, seguida de acidose, alterações visuais ("visão em nevada"), convulsões e coma.
- Crise no Brasil: entre setembro e novembro de 2025, o Brasil registrou 890 notificações de intoxicação por metanol em bebidas alcoólicas, das quais 73 casos foram confirmados em sete estados, resultando em 22 óbitos — com São Paulo concentrando cerca de 68% dos casos confirmados (50) e 10 das mortes.
- Alerta OPAS/OMS (out. 2025): envenenamentos em pelo menos cinco países das Américas, com mais de 200 casos suspeitos no Brasil por bebidas destiladas adulteradas [16].
- Tratamento: inibidores competitivos da ADH — etanol terapêutico ou, preferencialmente, fomepizol (ataque 15 mg/kg; manutenção 10 mg/kg a cada 12 h) [17–19].
- Agravantes na América Latina: fomepizol é caro e de baixa disponibilidade [19,20]; confirmação analítica por GC-FID / GC-MS é restrita a laboratórios oficiais, com tempos de resposta de horas a dias.
- 2026 balanço até 3 de fevereiro: continuidade da crise. 7 casos confirmados e 13 em apuração. Dois óbitos, um na Bahia e outro em São Paulo.
A conclusão prática é que o ganho clínico e epidemiológico mais alto não vem de tratar melhor quem já se intoxicou, e sim de impedir que a bebida adulterada chegue ao consumidor. Isso exige ferramentas de triagem rápidas, baratas e disponíveis em campo.
O estado atual da identificação e quantificação de metanol em bebidas e combustíveis
As técnicas analíticas disponíveis para identificação e quantificação de metanol em bebidas e combustíveis são, no essencial, as mesmas — mudam a norma que as regula (AOAC e farmacopeias nacionais para bebidas; ABNT NBR 16041 e Res. ANP 907/2022 para combustíveis) e os laboratórios ou agentes que as executam. A Tabela 1 abaixo organiza essas ferramentas pelo eixo que importa para saúde pública e fiscalização em campo: disponibilidade, investimento e custo por análise.
Tabela 1. Ferramentas analíticas para quantificação e/ou identificação de metanol em bebidas e combustíveis e a proposta do Alcolab.
| Método | Comentário | Disponibilidade e limitações | Investimento | Custo/análise |
|---|---|---|---|---|
| Cromatografias instrumentais (GC-FID e GC-MS) | Padrão-ouro confirmatório para bebidas (AOAC [21]) e combustíveis (ABNT NBR 16041 / Res. ANP 907/2022 [22,23]). | Muito baixa. Disponível apenas em laboratórios estruturados e grandes centros. Resposta: horas a dias. | Alto (> US$ 50 mil) | Intermediário (US$ 100–300) |
| Sensor quimiorresistivo portátil em ar exalado | Triagem da vítima já exposta, com boa correlação contra GC-MS (R² = 0,966) [24]. Não analisa a bebida nem o combustível em si. | Baixa (emergência clínica). Não aplicável à análise da amostra antes do consumo ou da entrega. Resposta: 2 min. | Intermediário (US$ 5 mil-15 mil) | Alto (US$ 100/teste) |
| Densímetro (termodensímetro, picnômetro, tubo em U oscilante) | Método clássico de alcoolometria em bebidas (OIML R 22 / AOAC [21,25,26]) e instrumento obrigatório da fiscalização da ANP em postos revendedores de etanol combustível [22,27]. | Média. Resposta: minutos. Limitação fundamental: ρ(MeOH) ≈ ρ(EtOH) — metanol é praticamente invisível ao densímetro até ~40 % de substituição. | Baixo a intermediário (< US$ 50 para termodensímetro de vidro; alguns milhares de dólares para densímetro de tubo em U oscilante) | Muito baixo (< US$ 1) |
| Técnicas espectroscópicas (NIR, FTIR-ATR, Raman) | LOD típico de 2,5–6 % m/m; existem versões portáteis comerciais, vantagem prática para fiscalização em campo [28–30]. | Baixa (operação especializada). Pode exigir calibração multivariada e matrizes bem comportadas. Resposta: 1–15 min. | Intermediário a alto (US 150 mil) | Baixo (US$ 3–15) |
| Colorimetria (permanganato / ácido cromotrópico / ISO 1388-8) | Triagem qualitativa de baixíssimo custo (ISO 1388-8 [22] para combustíveis; ácido cromotrópico / permanganato para bebidas). | Alta. Sujeita a interferências de matriz: congêneres naturais e pigmentos em destilados envelhecidos, licores e bebidas coloridas geram falsos positivos; amostras muito diluídas geram falsos negativos. Resposta: 5–15 min. | Muito baixo (< US$ 50, reagentes e vidraria) | Muito baixo (< US$ 1) |
| AlcoLab (densidade + viscosidade em seringa e balança) | Triagem qualitativa e semiquantitativa: detecta metanol acima de ~5 % m/m (LOD pode ser reduzido com recalibração) e estima a composição ternária água–etanol–metanol; gratuito, open source (AGPL-3.0), executa no navegador e funciona offline. Aplicável tanto a bebidas quanto a etanol combustível. | Alta (usuário final, fiscal, profissional de saúde pública). Resposta: 10–20 min. | Muito baixo (< US$ 30, seringa, balança, termômetro) | Baixíssimo (~US$ 0,00; não utiliza reagentes químicos e o padrão de calibração é a água) |
Em um extremo, a cromatografia é o padrão-ouro — precisa, exata, regulatoriamente aceita para autuação administrativa e judicial — mas restrita a laboratórios oficiais, com tempo de resposta em horas a dias que não serve à decisão rápida em campo. No extremo oposto, a colorimetria é barata e imediata, mas sofre interferências de matriz que comprometem seu uso em destilados envelhecidos, licores, bebidas coloridas e amostras muito diluídas. Entre os dois, as técnicas espectroscópicas portáteis (NIR, FTIR, Raman) oferecem um compromisso interessante, mas ainda operam em faixa de dezenas a centenas de milhares de dólares e podem exigir calibração multivariada específica para cada matriz.
No lado clássico da fiscalização, o densímetro — instrumento obrigatório da ANP em postos revendedores e método centenário de alcoolometria em bebidas — tem uma limitação fundamental: é incapaz de detectar metanol enquanto a substituição se mantém abaixo de ~40%, porque ρ(MeOH) ≈ ρ(EtOH). O sensor quimiorresistivo em ar exalado, por sua vez, triage a vítima já exposta, não a amostra antes do consumo ou da entrega.
A lacuna é evidente e simétrica nos dois domínios: falta uma ferramenta que o usuário final, o fiscal ou o profissional de saúde pública possa usar em campo, sem reagentes, com custo na casa de algumas dezenas de reais, para triar bebida ou combustível antes que a amostra chegue ao consumidor ou ao tanque. É nessa lacuna que o AlcoLab se insere — com o mesmo método físico (densidade + viscosidade) aplicável aos dois contextos.
Densidade: forte para quantificar álcool, insuficiente para discriminar metanol
Por que a densidade funciona tão bem para soluções hidroalcoólicas
A densidade de uma mistura líquida depende do volume molar dos seus componentes e das interações moleculares entre eles. Para o sistema binário água-etanol, a dependência da densidade com o teor alcoólico é monotônica e suave entre 0 e 100 % de etanol. Essa robustez explica por que a densitometria é o método universal de quantificação de etanol em bebidas há mais de um século [21,25,26], e é também o motivo pelo qual a ANP, na Resolução nº 907/2022, adota a massa específica a 20 °C como um dos importantes parâmetros físico-químicos de qualidade do etanol hidratado combustível (EHC), com faixa especificada de 807,6 a 811,0 kg/m³ [22,27].
As compilações de referência seguem três linhagens: (i) metrológica europeia — tabelas de Osborne, McKelvy e Bearce (1913), adotadas pela OIML na recomendação OIML R 22 (International Alcoholometric Tables); (ii) compêndios AOAC International e farmacopeias nacionais (USP, Farm. Bras., EP), ajustados a ±0,01 °GL para fins regulatórios; (iii) modelos preditivos calibrados com densímetros de tubo em U oscilante (Anton Paar DMA 4500/5000/5001), em que desvios de 0,00002 g/cm³ propagam-se em ±0,01 %m/m de etanol [28,31,32].
Em equipamento de rotina, três instrumentos dominam o cenário:
- Alcoômetros e picnômetros de vidro: custo baixíssimo, mas exatidão limitada (±0,5 °GL em alcoômetros comerciais).
- Densímetros portáteis de tubo em U oscilante: exatidão ≈ 0,001 g/cm³, custo USD 3000–15000.
- Densímetros de bancada Anton Paar: padrão metrológico (±0,00005 g/cm³), inviáveis fora de laboratório.

Para o AlcoLab, a exigência não é exatidão metrológica absoluta, e sim uma densidade relativa ρ/ρ_H₂O bem estimada a partir de um densímetro comum ou de pesagem simples em balança com resolução 0.1g (podendo ser até de uso doméstico). É o suficiente para restringir a busca ternária por viscosidade, como se verá adiante.
Por que a densidade, sozinha, não basta para metanol — e consequência para a triagem
Considere as densidades absolutas puras a 20 °C: g/cm³; g/cm³; g/cm³. O contraste entre os dois álcoois é de apenas g/cm³ ( %), muito abaixo do limite de detecção de qualquer densímetro doméstico e mesmo abaixo da precisão típica de densímetros portáteis de ±0,001 g/cm³.
Formalmente, trata-se de um problema de não-injetividade: seja na região típica de destilados ( entre 0,25 e 0,50), seja no regime do EHC ( ≈ 0,93), a densidade da mistura é praticamente independente da fração interna entre os dois álcoois. Há, portanto, infinitas composições (, ) que produzem a mesma densidade. Uma mistura água-etanol de 40 % m/m é densimetricamente indistinguível de uma mistura água-metanol de 40 % m/m pela grande maioria das técnicas por densidade; no EHC, cenários de adulteração com até ~20 % de substituição por metanol produzem variação de densidade inferior à resolução de um termodensímetro de campo e da própria tolerância especificada pela ANP [22].
Estudos de referência [28,31] reforçam esse limite: trabalhos sobre densidade e volumes molares de excesso em misturas ternárias água-metanol-etanol [33] mostram que a diferença entre os excessos água-etanol e água-metanol produz uma assinatura tênue demais para servir de vetor discriminatório em instrumento de baixo custo.
Consequência prática: a densitometria clássica, apesar de seu mérito inquestionável na quantificação de etanol, nunca foi adotada como ferramenta de triagem de metanol — seja em bebidas, seja em combustíveis. A literatura de adulteração reconhece há décadas essa lacuna e recomenda, para esse fim, métodos cromatográficos confirmatórios ou como mais acessíveis e portáveis as técnicas espectroscópicas (NIR, FTIR-ATR, Raman) [28–30], que, embora portáteis, têm custo de aquisição elevado e raramente estão disponíveis para fiscalização municipal ou para inspeção rotineira em postos revendedores. Faltava a combinação de uma segunda grandeza física, que a metodologia aqui proposta [e embarcada no AlcoLab] introduz na forma da viscosidade relativa medida em seringa com agulha 22G. A densidade, longe de ser abandonada, assume papel fundamental: restringe drasticamente a região do espaço de composições em que a amostra pode estar, direcionando a busca pela viscosidade.
Viscosidade: a grandeza que separa metanol de etanol
Diante da inviabilidade de usar apenas a densidade, os autores iniciaram uma investigação sistemática de propriedades físicas simples, mensuráveis em campo, que discriminassem os dois álcoois. A viscosidade emergiu como a candidata natural.
A viscosidade dinâmica μ é, em termos macroscópicos, a resistência ao escoamento sob tensão de cisalhamento; microscopicamente, é determinada pela frequência de saltos moleculares e pela eficiência do empacotamento. Os valores puros a 20 °C são:
- mPa·s
- mPa·s
- mPa·s
O contraste entre os dois álcoois é enorme: é mais de duas vezes . Essa diferença não é acidental — reflete a forte contribuição do grupo metila adicional do etanol à energia de ativação do escoamento (dominada por interações dispersivas C–H⋯H–C e por volume livre menor). A viscosidade oferece, portanto, um fator de discriminação muito superior ao da densidade, tanto no regime dos destilados quanto no regime do etanol combustível.
O desvio da viscosidade em misturas aquosas
Quando os álcoois são misturados à água, a viscosidade não se comporta de maneira simples. Para os dois binários de interesse — água-metanol e água-etanol — a viscosidade passa por um máximo acentuado em composição intermediária: cerca de ≈ 0,65–0,75 para água-etanol ( ≈ 2,5–2,9 mPa·s) e ≈ 0,70 para água-metanol ( ≈ 1,5–1,7 mPa·s), como se observa no gráfico abaixo. O desvio positivo em relação à média ponderada é manifestação direta da reorganização da rede de pontes de hidrogênio: a água se estrutura ao redor das cadeias alifáticas do álcool (clusters hidrofóbicos), criando arranjos metaestáveis que aumentam a fricção [33–36]. Acima de ~50 % m/m de álcool, a estrutura da água é progressivamente desmontada e a viscosidade decresce.
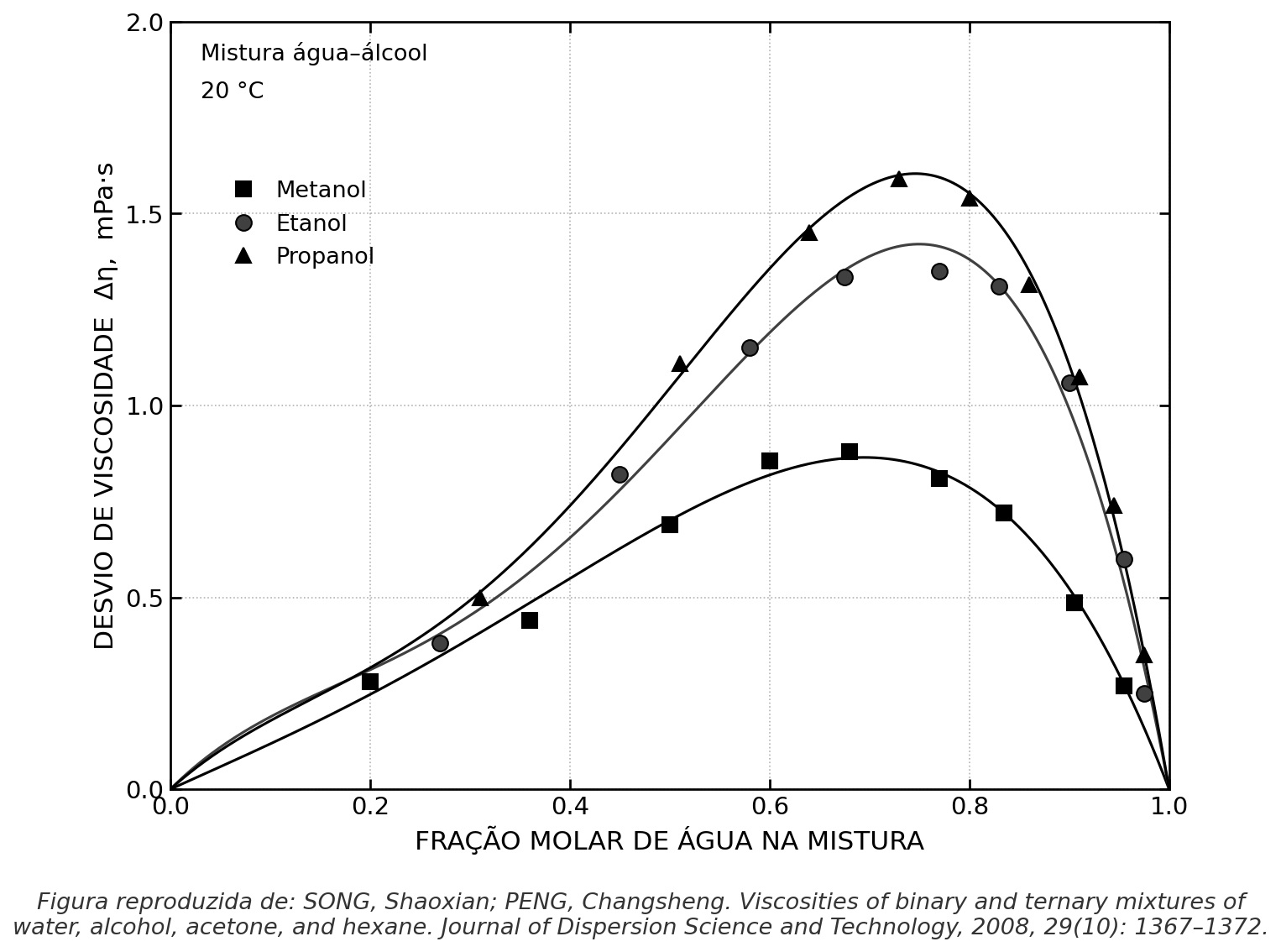
Apesar desse comportamento não ideal, a grande diferença absoluta entre etanol e metanol puros mantém a discriminação em misturas. Uma mistura água-etanol a 40 % m/m exibe viscosidade próxima de 2,5 mPa·s a 20 °C, enquanto uma mistura água-metanol na mesma proporção fica em torno de 1,5 mPa·s — uma diferença de quase 70 %. Isso se traduz em tempos de escoamento bem distintos no mesmo sistema capilar. O mesmo princípio se aplica a misturas ternárias: duas amostras com a mesma fração total de álcool, mas com predominância de etanol em uma e de metanol na outra, apresentarão tempos de escoamento marcadamente diferentes — seja no regime de bebidas destiladas (0,25 ≲ ≲ 0,50), seja no regime do EHC ( ≈ 0,93). É essa separação que o AlcoLab explora.
O AlcoLab: proposta, autores, princípio de funcionamento
O AlcoLab é uma ferramenta web gratuita, open-source e offline-capable, desenvolvida pelos autores Diego Mendes de Souza, Pedro Augusto de Oliveira Morais e Nayara Ferreira Santos. O aplicativo executa o pipeline analítico inteiramente no navegador via Pyodide (Python compilado para WebAssembly), sem envio de dados a servidores, e funciona em qualquer smartphone atual.
Insumos físicos necessários:
- uma seringa comercial descartável de 20 mL com agulha 22G (o tipo mais comum em farmácias);
- uma balança com resolução mínima de 0,1 g (pode ser substituído por um densímetro);
- um smartphone;
- um termômetro, seu uso pode ser dispensado pela estabilização da temperatura da amostra e da água.

Princípio: a análise combina duas grandezas físicas complementares.
- A densidade relativa — obtida diretamente por densímetro ou pela pesagem de um volume calibrado da amostra contra água — fornece o teor alcoólico total (w, fração mássica de álcool) com precisão suficiente para restringir a região do espaço de composições em que a amostra se encontra.
- A viscosidade aparente relativa — obtida pelo tempo de escoamento gravitacional pela seringa — fornece uma segunda grandeza que, diferentemente da densidade, discrimina metanol e etanol.
A combinação das duas permite estimar a composição ternária água-etanol-metanol mais compatível com as medidas e, em consequência, identificar amostras com metanol acima de um limiar de segurança. O mesmo princípio se aplica tanto à triagem de bebidas destiladas quanto à triagem de etanol combustível.
A densidade diz quanto álcool há ao todo; a viscosidade diz que álcool é ou a contribuição de cada um.
Passo a passo analítico do AlcoLab
Entrada e normalização
O fluxo começa com o perfil do usuário (leigo, técnico ou laboratório), que adapta a granularidade da interface, e com os metadados da amostra (tipo, teor de rótulo em °GL / %v/v / %m/m, marca, lote). A validação é feita por schema Zod que rejeita valores fora de ranges físicos plausíveis. Internamente, toda composição passa a ser expressa em fração mássica e toda temperatura em °C. A conversão %v/v → %m/m usa tabela interpolada a 20 °C (conversao_vv_para_wE_20C.csv); bebidas ou amostras de EHC rotuladas em °GL / °INPM a temperatura ≠ 20 °C passam primeiro por correção via densidade_alcool_gl20a30.csv.
Medição de densidade (Fluxo 1)
- Tarar a balança com a seringa vazia (ou registrar e subtrair).
- Aspirar exatamente 20,0 mL de água; pesar; registrar .
- Aspirar exatamente 20,0 mL da amostra (após enxágue com a própria amostra); pesar; registrar .
Densidade relativa: . Com balança de 0,1 g, a incerteza típica é ±0,005 em , equivalente a ±0,5–1 % em teor alcoólico em massa — suficiente para o papel da densidade no método (direcionar a busca na malha de viscosidade, não quantificar álcool com precisão metrológica).
A conversão → w_álcool faz busca inversa simultânea nas malhas binárias EtOH–H₂O e MeOH–H₂O a 20 °C, retornando (w_EtOH_equiv, w_MeOH_equiv). A média é usada como estimativa pontual de e o intervalo entre os dois valores fornece a faixa possível — abordagem deliberadamente conservadora dada a quase coincidência das duas curvas binárias.
Medição de temperatura
O usuário registra a temperatura da água e da amostra, podendo distinguir em até 3ºC (app faz correção da viscosidade em função da temperatura entre 20 e 30ºC). Pode optar por não registrar desde que garanta equalização de temperatura entre água e amostra. Neste caso, o software orienta o usuário ao tempo mínimo para se atingir a estabilidade térmica.
Medição de viscosidade (Fluxo 2)
O usuário cronometra dois (ou mais) tempos de escoamento de um volume fixo (padrão 10 mL) da água e da amostra na mesma seringa+agulha. O app calcula o CV entre repetições; se CV > 5%, alerta e recomenda repetir. Os tempos médios alimentam um pipeline de três etapas (viscosidade absoluta aparente por Hagen–Poiseuille → correção relativa à água → normalização térmica para 20 °C) que resulta na viscosidade da amostra corrigida e referenciada a 20 °C, pronta para consulta na malha.
Densidade como "norte" para viscosidade: por que é o ponto-chave
A malha ternária do AlcoLab é uma superfície curva em (, ). A Figura 1 mostra um corte dessa malha a 20 °C, com a viscosidade no eixo vertical e a fração mássica total de álcool no eixo horizontal.
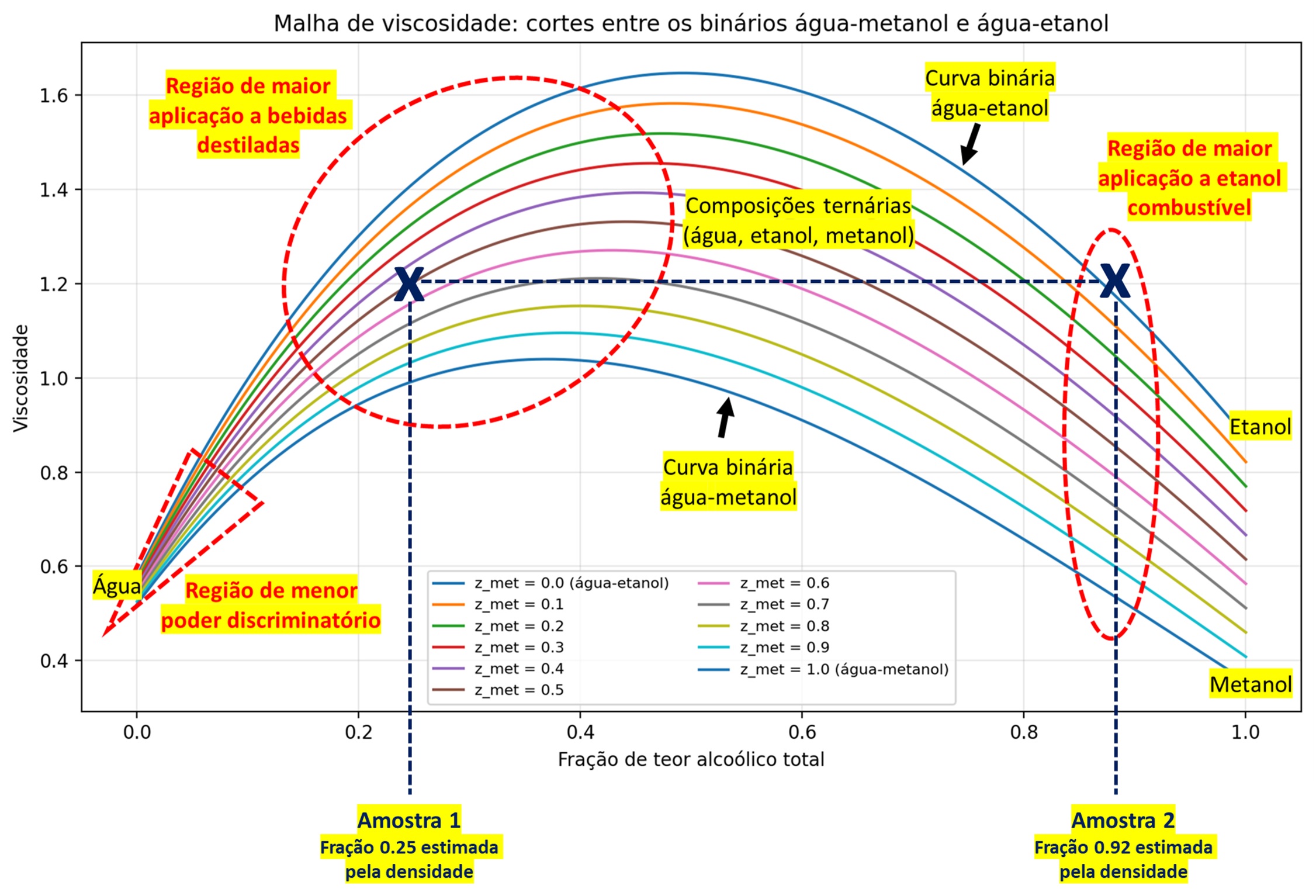
Como ler a figura. As curvas representam, de cima para baixo:
- A curva no topo () é o binário água-etanol: vai do ponto "Água" na origem (à esquerda, onde μ ≈ 1,0 mPa·s) até o ponto "Etanol" no canto direito superior.
- A curva na base () é o binário água-metanol: parte do mesmo ponto "Água" e termina no ponto "Metanol" no canto direito inferior, com viscosidade sensivelmente menor que o etanol puro.
- Entre as duas, nove curvas intermediárias ( a ) descrevem misturas ternárias água–etanol–metanol com proporção crescente de metanol no álcool total. Todas partem do mesmo ponto (água pura) e vão se separando à medida que o teor alcoólico aumenta, refletindo a diferença de viscosidade entre os dois álcoois puros discutida na seção anterior.
Três regiões em destaque na figura.
- Região de menor poder discriminatório (elipse à esquerda, ≲ 0,10): as curvas estão praticamente superpostas — há pouca diferença prática e numérica entre as curvas binárias água-etanol, água-metanol e todas as possibilidades ternárias. Na prática, fica estatisticamente difícil distinguir se apenas um álcool presente ou qual proporção de cada um. Por isso, em amostras muito diluídas é comum os resultados demonstrarem diferentes composições em termos de participantes (água e um dos álcoois, e uma composição ternária) são possíveis e estatisticamente equivalentes.
- Região de maior aplicação a bebidas destiladas (elipse central, ≈ 0,25–0,50): destilados típicos (cachaça, vodka, gim, whisky) ficam nessa faixa, em que a separação vertical entre as curvas é muito satisfatória (maior poder discriminante).
- Região de maior aplicação a etanol combustível (elipse à direita, ≈ 0,90–0,95): concentra o EHC, onde a separação entre as curvas também é muito satisfatória e, portanto, suficiente para discriminar adulterações ≳ 5 % de metanol.
O problema da ambiguidade da viscosidade - e como a medida de densidade o resolve. Imagine uma medida experimental de viscosidade mPa·s (linha horizontal tracejada na figura). Se apenas a viscosidade fosse consultada, a malha ofereceria duas soluções plausíveis completamente opostas, marcadas com X:
- Amostra 1, à esquerda: ≈ 0,25, sobre a curva marrom ( intermediário) — caracterizaria uma bebida destilada de teor médio que sofreu adulteração e apresenta metade do alcool total como etanol e outra metade metanol.
- Amostra 2, à direita: ≈ 0,92, sobre uma curva alta ( alto) — caracterizaria um etanol combustível não adulterado.
São composições quimicamente opostas, em domínios analíticos opostos, mas produzem o mesmo tempo de escoamento pela seringa por apresentarem mesma viscosidade. A viscosidade sozinha não resolveria; a densidade sozinha também não — como visto na seção sobre densidade, o contraste de 0,26 % entre os dois álcoois puros está abaixo da resolução de qualquer balança doméstica.
É justamente da combinação das duas que nasce uma decisão mais discriminatória na identificação da composição hidroalcoólica. A densidade atua como filtro de região: a pesagem simultânea do volume calibrado informa a priori, com incerteza típica de ±1–3 %. O AlcoLab, por construção, restringe a busca na malha a uma janela de ±3 % em torno do estimado pela densidade. As duas hipóteses acima, portanto, não se confundem: se a densidade aponta para a vizinhança da Amostra 1, toda a região da Amostra 2 é descartada de imediato (e vice-versa). Só depois desse filtro a viscosidade é consultada, para escolher — dentro da janela compatível — qual composição explica melhor .
No caso específico do EHC, é conhecido a priori por especificação regulatória (cerca de 0,93) e o filtro de densidade atua com ainda mais força: a busca fica restrita à faixa direita do gráfico, e a viscosidade fica exclusivamente encarregada de estimar a fração de metanol no álcool total.
Cálculo e exibição
O Web Worker carrega o runtime Pyodide (5–10 s na primeira chamada) e executa: (i) app_w_alcool_v2.py → a partir da densidade; (ii) main.py + processamento.py → pipeline de correção, consulta à malha, composição ternária mais compatível e análise estatística. O resultado é serializado para exibição em results/page.tsx.
A camada estatística do AlcoLab
Por que uma camada estatística específica é necessária
A saída bruta do pipeline é a "composição mais compatível" com (, μ_relativa). Não basta: o usuário final precisa saber se (i) essa composição é estatisticamente melhor que a hipótese "sem metanol" e (ii) quão confiável é essa decisão frente à incerteza das medidas em seringa e balança.
O AlcoLab responde à primeira pergunta com um teste t-Student bilateral e à segunda com uma simulação de Monte Carlo com 3 000 replicatas.
Métodos
Teste t-Student / Welch [37]. Para n ≥ 2 repetições:
Decisão bilateral com α = 0,05; rejeita (mistura idêntica à referência) se |t| excede . Com n = 1, o app cai em aproximação normal (z-score) com SD default = 0,025 mPa·s relativo. Correção de Welch é invocada automaticamente quando há heterocedasticidade forte entre amostra e referência [38,39].
Monte Carlo para propagação de incerteza. Formalizada em GUM S1 [40–42], é o padrão quando (a) a relação entrada/saída é fortemente não-linear ou (b) as distribuições não são gaussianas. Ambas as condições se aplicam: a malha é não-linear em (w, z) e a medida em seringa tem distribuição aproximadamente normal mas com caudas por falhas operacionais pontuais. Estudos comparando GUM analítico com MC [41,42] mostram que em problemas multivariados não-lineares o MC captura covariâncias e assimetrias que o GUM linearizado subestima; aplicações em copulas [43] e forense [44] validam a abordagem. 3 000 replicatas rodam em < 1 s em navegador moderno.
Implementação e hipóteses comparadas
Parâmetros fixados em código: MC_N_DEFAULT = 3000; ALPHA_MEDIA = 0,05; P_CUTOFF_HIGH_SELECTIVITY = 0,70; P_CUTOFF_LOW_SELECTIVITY = 0,80; W_LOW_SELECTIVITY = 0,20; SD_DEFAULT_N1 = 0,025; MALHA_SIGMA_DEFAULT = 0,0 (reservado para um σ por célula futuro).
O núcleo de _avaliar_amostra gera mu_sims = N(μ_mean, μ_se, size=3000) e, para cada hipótese H_k, calcula contra a viscosidade prevista pela malha. A hipótese vencedora por replicata é contada; a probabilidade posterior é a fração de vitórias. A semeadura do RNG é feita por CRC32 do identificador da amostra, garantindo reprodutibilidade cross-platform (importante para auditabilidade em perícia).
Hipóteses comparadas em paralelo (dentro da faixa de direcionada pela densidade):
- : composição ternária mais compatível (permite todos os três componentes);
- : binário água-etanol ( = 0);
- : binário água-metanol ( = 1);
- : traços (1–5 % m/m) de um álcool no outro — para capturar adulteração leve.
Decisão conservadora:
- Se ≥ → "compatível com etanol apenas".
- Se ≥ e na composição mais compatível > 5 % m/m → "incompatível" (provável adulteração).
- Casos intermediários → amarelo, recomenda repetir.
Sensibilidade efetiva por faixa
Em ≤ 0,20 as duas bordas binárias se aproximam (ambas tendem a μ da água), e o teste fica naturalmente menos seletivo. O app eleva o cut-off de 0,70 para 0,80 e inclui hipóteses de traços 1–5 %. Resultado prático:
- 0,30–0,60 (destilados típicos — cachaça, vodka, gim, whisky): sensibilidade a ≥ 5 % com confiança ≥ 70 %.
- 0,15–0,30 (licores, cervejas fortes): sensibilidade a ≥ 10 % com confiança ≥ 80 %.
- < 0,15 (bebidas muito diluídas): "álcool detectado, discriminação inconclusiva"; recomenda análise complementar.
- ≈ 0,93 (etanol hidratado combustível): regime de alto teor, com as duas bordas binárias ainda suficientemente separadas em viscosidade — sensibilidade compatível com a detecção de ≥ 5–10 %, faixa que abrange todos os cenários documentados na Operação Carbono Oculto (20–90 % de metanol).
Semáforo final
Integra três blocos em semaphoreLogic.ts:
- Qualidade experimental (
experimentApproved): ≥ 2 repetições, CV ≤ 5 %, se houver vídeo+IA, μ da água de referência dentro de ±15 % do tabelado. - Compatibilidade analítica (
compativel): Compatible / Incompatible / Inconclusive. - Semântica por tipo de amostra (bebida vs. álcool comercial vs. etanol combustível): para bebidas, vermelho exige ambos "Incompatible" E "metanol alto (> 5 %)" E
experimentApproved; para EHC, a mesma lógica se aplica usando o limite regulatório da ANP (0,5 % v/v) como gatilho de vermelho quando a medida estatisticamente excede esse valor.
Por construção, é conservadora: vermelho só dispara quando a evidência experimental é boa, a decisão estatística é robusta e o contexto permite conclusão toxicologicamente ou regulatoriamente relevante. Amostras borderline caem em amarelo.
Discussão e limitações
Desempenho atual
Em testes de validação com amostras preparadas em laboratório com concentrações conhecidas:
- Quantificação de : erros típicos < 5 % em 0,25 ≤ ≤ 0,70.
- Identificação de metanol > 5 % m/m em amostras com ≥ 0,30: taxa de acerto 100 % nos conjuntos internos.
- Falsos positivos em amostras legítimas: próximos de zero, graças ao semáforo conservador.
- Aplicabilidade a etanol combustível: o princípio físico é o mesmo — validação formal em amostras reais de EHC, em conjunto com a ANP e laboratórios credenciados, é um dos próximos passos do projeto.
Por que o limiar de 5 % é clinicamente adequado em bebidas
Não é uma limitação acidental: as intoxicações graves relatadas envolvem tipicamente bebidas com 10–40 % m/m de metanol, associadas a adulterações grosseiras para aumentar rendimento de destilados [14,15,45,46]. Em quantidades pequenas (< 1–2 %), o metanol compete com o etanol pela ADH: se o etanol está muito acima do metanol, o fígado processa preferencialmente o etanol e parte do metanol é eliminado inalterado antes da formação tóxica de formiato [17,47]. Além disso, traços de 0,1–1 % m/m ocorrem naturalmente em destilados de frutas (aguardentes, bagaceiras, grappas) e são legalmente permitidos (Regulamento UE 2019/787). O AlcoLab é projetado para o perfil de risco que importa — fraudes com substituição significativa — e não para quantificar traços inofensivos.
No caso do etanol combustível, o limite regulatório é ainda mais estreito (0,5 % v/v pela Res. ANP 907/2022 [22]). O AlcoLab não pretende competir com a GC-FID na verificação desse limite regulatório nominal, mas sim fornecer triagem rápida de campo em cenários de adulteração grosseira — como os 20–90 % documentados na Operação Carbono Oculto [7,8] — que são, de longe, os de maior impacto sanitário e econômico.
Limitações remanescentes
- Faixa de temperatura de operação (20–30 °C): fora dela, análise de viscosidade desabilitada; recomenda-se aguardar equilíbrio térmico.
- Poucos pontos experimentais no interior do simplex ternário: MAPE 4–8 % na validação externa é aceitável para triagem, não para metrologia de alta exatidão. Expandir o conjunto é o caminho mais imediato de refinamento.
- Regiões de baixa seletividade ( < 0,20) e bordas extremas ( > 0,80): resolução discriminatória menor; tendência a "inconclusivo". Um acréscimo futuro pode ser confirmação colorimétrica rápida (ácido cromotrópico) nessas regiões específicas.
- Validação formal em EHC: conduzida em parte pelos autores mas ainda pendente de estudo interlaboratorial com amostras reais de postos revendedores, em parceria com a ANP.
Como o AlcoLab foi disponibilizado: licença AGPL-3.0 e estratégia de abertura
Quando a metodologia já estava estruturada e os testes experimentais confirmavam o potencial da ferramenta, a equipe enfrentou uma decisão concreta: pedir patente — processo de 2 a 7 anos, com proteção da invenção e possível retorno — ou lançar imediatamente, de graça, assumindo os custos do próprio bolso, sem garantia alguma de retorno. Havia surto ativo de intoxicações no Brasil e em outros países, vidas em risco, e uma janela de tempo que a via patentária não conseguiria atender. A equipe escolheu lançar. O AlcoLab foi ao ar em 10 de março de 2026.
A escolha por AGPL-3.0
O AlcoLab foi publicado sob licença GNU AGPL-3.0 — uma das licenças de código aberto mais rigorosas disponíveis. A propriedade central da AGPL, relevante para uma ferramenta de saúde pública e de apoio à fiscalização de combustíveis, é o chamado "copyleft de rede": qualquer versão modificada do código — inclusive versões executadas como serviço web por terceiros — precisa disponibilizar publicamente o código-fonte modificado. Isso impede que um ator privado pegue o AlcoLab, faça melhorias e as transforme em produto proprietário pago, sem devolver à comunidade o que derivou do trabalho aberto.
Na prática, a AGPL-3.0 garante três coisas ao ecossistema de saúde pública e de fiscalização:
- A gratuidade é juridicamente sustentável. Uma empresa pode usar o AlcoLab comercialmente, mas se o modificar para oferecer um serviço, deverá publicar a versão modificada sob a mesma licença.
- A metodologia continua auditável. Pesquisadores, peritos, fiscais e agentes de saúde pública podem revisar o algoritmo, validar critérios estatísticos e propor melhorias — condição essencial quando se trata de decisão que afeta consumo de bebida ou comercialização de combustível.
- A ferramenta pode ser adaptada a outros contextos (outros tipos de amostra, outras línguas, outras interfaces) desde que se mantenha o compromisso de abertura.
Por que os autores optaram por essa abordagem
A equipe identificou três razões convergentes:
- Urgência de saúde pública. Dezenas de casos no Brasil em 2025 e o alerta da OPAS/OMS em outubro de 2025 [16] tornavam a janela patentária inviável eticamente.
- Alinhamento com o público-alvo. A ferramenta faz mais sentido exatamente em regiões com pouca infraestrutura laboratorial — onde um produto proprietário teria adoção muito menor.
- Auditabilidade como requisito técnico. Para uma ferramenta cujo resultado pode orientar consumo, denúncia, autuação ou apreensão de combustível, metodologia fechada é obstáculo científico, não vantagem competitiva.
Proteção da prioridade e publicação científica
Abertura não significa ausência de proteção da autoria. Antes da publicação pública, a equipe executou dois passos estratégicos:
- Depósito junto ao INPI, fixando a data de prioridade da invenção no Brasil.
- Publicação no Zenodo, repositório científico internacional com DOI permanente.
Esses registros não visam exploração comercial — visam justamente o contrário: impedir que um terceiro reivindique a ideia como própria depois que ela já foi tornada pública. É uma proteção orientada à abertura, não ao fechamento. O código completo está em github.com/diegoanapolis/alcolab.
Primeiros resultados de adoção
Em cerca de um mês de site público, o AlcoLab registrou quase 2 500 visitantes únicos e aproximadamente 34 000 requisições ao servidor, com acessos em todos os continentes — Brasil, Estados Unidos, China, França, Canadá, Singapura e Suíça, entre outros. A adesão internacional confirma o que a equipe suspeitava: a contaminação por metanol não é um problema exclusivamente brasileiro; é global, especialmente em países com fiscalização e infraestrutura laboratorial limitadas, e atinge tanto bebidas quanto combustíveis.
Parcerias necessárias e riscos ao projeto
O custo real da gratuidade
Software gratuito não é software sem custo — significa que alguém está arcando com ele. No caso do AlcoLab, essa conta foi — e continua sendo — paga pelos próprios criadores: hospedagem em servidor, registro de domínio, bebidas comerciais para testes, materiais de calibração, reagentes e muitas horas de pesquisa e desenvolvimento. Os custos estimados até a publicação deste texto estão na Tabela 2.
Tabela 2. Custos estimados do projeto AlcoLab custeados pelos autores (até abril/2026).
| Item | Detalhe | Custo estimado |
|---|---|---|
| Bebidas para calibração | 10 rótulos (whisky e vodka) | R$ 1 000 |
| Reagentes químicos | Etanol e metanol P.A., 10 L cada | R$ 1 600 |
| Infraestrutura — Railway Pro | US$ 20/mês \times 6 meses | R$ 700 |
| Ferramentas de desenvolvimento | GitHub Copilot + Claude Max, 6 meses | R$ 3 840 |
| Horas de P&D | 290 h (Diego 150h · Pedro 80h · Romério 30h · Nayara 30h) | R$ 29 000 |
| Total investido estimado | R$ 36 140 |
Riscos reais de um projeto sem suporte institucional
Projetos open source sem apoio institucional têm um histórico conhecido: desenvolvedores voluntários se sobrecarregam, manutenção se acumula, atualizações deixam de ser feitas e a infraestrutura vai ficando vulnerável. O resultado é o que o meio chama de abandonware — software que existe, mas não tem mais ninguém por trás. Para uma ferramenta de saúde pública e de apoio à fiscalização de combustíveis, esse desfecho é particularmente grave: a continuidade depende de manutenção ativa (atualização de dependências, correções de segurança, novos pontos de calibração, adaptação a novos tipos de bebida ou de combustível). É esse cenário que a equipe quer evitar — precisamente porque acredita no impacto positivo da ferramenta.
Parcerias com laboratórios oficiais
A primeira frente de parcerias buscada é com laboratórios oficiais de metrologia legal e institutos de pesquisa — ANP, ANVISA, MAPA, INMETRO no Brasil, equivalentes em outros países. O objetivo é:
- Aumentar o número de pontos de calibração no interior do simplex ternário, substituindo parte da derivação RK-mid por medidas experimentais diretas e refinando o termo de excesso em toda a faixa de , inclusive na região do EHC.
- Conduzir estudos de precisão interlaboratorial e entre analistas, quantificando a reprodutibilidade real do método em condições de fiscalização.
- Aumentar a robustez e a confiabilidade da malha experimental, devolvendo ao usuário final resultados mais assertivos e estatisticamente qualificados.
Parcerias com instituições de fiscalização
A segunda frente é com instituições relacionadas à fiscalização de bebidas e combustíveis — Vigilância Sanitária, Polícia Civil, Procon, MAPA, ANP, Anvisa. O objetivo aqui é bidirecional: (i) disponibilizar a ferramenta validada a agentes de campo como triagem pré-laboratorial, tanto em bebidas quanto em postos revendedores de etanol combustível; (ii) captar dos próprios usuários finais as demandas reais — ajustes necessários, novas funcionalidades, tipos de amostra ainda não cobertos (licores, cervejas, vinhos, bebidas mistas, gasolinas), melhorias de usabilidade e integração com sistemas oficiais de notificação e com o PMQC. O ciclo de feedback com quem usa é o caminho mais curto para que o AlcoLab deixe de ser uma prova de conceito bem-sucedida e se torne um instrumento operacional da fiscalização brasileira e latino-americana.
Outras frentes em tratativa
No âmbito internacional, foram contatados os Médicos Sem Fronteiras (que mantêm a Methanol Poisoning Initiative desde 2012), a OPAS/OMS, fundações como Wellcome Trust e Gates Foundation, e organismos como BID Lab e STDF. No âmbito nacional, a lista inclui Fiocruz, MAPA, ANP, Vigilância Sanitária e parlamentares. No campo do fomento à pesquisa, há submissões planejadas à FAPEMA, FINEP e FAP-DF, além de FAPESP, CNPq e Finep para estudos de validação em larga escala.
Nenhuma parceria está fechada ainda — o projeto é recente e as tratativas estão em curso. O que existe de concreto é a ferramenta em si: funcional, gratuita, auditável, disponível agora. A consolidação, universalização e disseminação dependem daqui em diante do ecossistema institucional que conseguir se formar em torno dela.
Conclusão
O AlcoLab combina densidade e viscosidade — duas grandezas físicas simples, mensuráveis em campo com seringa, balança de cozinha e smartphone — em um pipeline analítico com camada estatística Monte Carlo, atingindo erros < 5 % em teor alcoólico total e identificação consistente de metanol acima de 5 % m/m, faixa compatível com o perfil clínico das intoxicações reais e também com os cenários de adulteração grosseira documentados em etanol combustível. A malha de viscosidade foi construída experimentalmente pelos autores no mesmo sistema seringa+agulha 22G usado pelo usuário final, após a constatação de que dados da literatura — medidos em viscosímetros padronizados — não transferiam para o escoamento gravitacional em seringa descartável. A ferramenta é gratuita, open source sob AGPL-3.0, e seu código é auditável em github.com/diegoanapolis/alcolab. A sustentabilidade e a universalização — tanto na triagem de bebidas quanto na triagem de combustíveis — dependem agora de parcerias técnicas e institucionais que os autores não têm capacidade de financiar isoladamente.
Para apoiar, colaborar ou demandar adaptação: [[email protected]](mailto:[email protected]) — e compartilhar com quem possa se beneficiar (consumidores, produtores, fiscais, agentes de saúde, reguladores de combustível) é, sempre, a forma mais simples de ajudar.
AlcoLab está disponível em alcolab.org.Código-fonte: github.com/diegoanapolis/alcolab · AGPL-3.0
Contato para parcerias: [email protected]
Referências
1. Gazeta do Povo. 2025. [Link](https://www.gazetadopovo.com.br/brasil/falsificacao-metanol-bebidas-combustiveis-convergem-com-rastro-de-mortes-feridos-milhoes-prejuizo/)
2. 2025. [Link](https://www.gov.br/saude/pt-br/assuntos/noticias/2025/dezembro/com-a-reducao-de-novos-casos-governo-do-brasil-encerra-sala-de-situacao-sobre-intoxicacao-por-metanol)
3. UNICA. 2026. [Link](https://unicadata.com.br/)
4. ANP. Programa de Monitoramento da Qualidade dos Combust\'\iveis –- PMQC. 2026. [Link](https://www.gov.br/anp/pt-br/assuntos/qualidade-de-produtos/programas-monitoramento/programa-de-monitoramento-da-qualidade-dos-combustiveis)
5. Argus Media. Viewpoint: Brazil methanol market adapts to spot price. 2025. [Link](https://www.argusmedia.com/en/news-and-insights/latest-market-news/2771339-viewpoint-brazil-methanol-market-adapts-to-spot-price)
6. NovaCana. 2025. [Link](https://www.novacana.com/noticias/mp-identificou-importacao-irregular-metanol-pcc-adulterar-combustiveis-280825)
7. DatamarNews. Brazil Cracks Down on Fuel Fraud Scheme Linked to PCC, Illegal Methanol Imports Through Paranaguá Port. 2025. [Link](https://datamarnews.com/noticias/brazil-cracks-down-on-fuel-fraud-scheme-linked-to-pcc-illegal-methanol-imports-through-paranagua-port/)
8. Combust\'\ivel do PCC tinha até 90\% de metanol; ANP permite só 0,5\%. 2025. [Link](https://visaoagro.com.br/combustivel-do-pcc-tinha-ate-90-de-metanol-anp-permite-so-05/)
9. Pohanka M. Antidotes Against Methanol Poisoning: A Review. Mini-Reviews in Medicinal Chemistry. 2019;19(14):1126–1136.
10. McMartin KE, Jacobsen D, Hovda KE. Antidotes for poisoning by alcohols that form toxic metabolites. British Journal of Clinical Pharmacology. 2015;81(3):505–515.
11. McMartin KE, Jacobsen D, Hovda KE. Antidotes for poisoning by alcohols that form toxic metabolites (updated review). British Journal of Clinical Pharmacology. 2024;90(9):2077–2088.
12. Rietjens SJ, de Lange DW, Meulenbelt J. Ethylene glycol or methanol intoxication: which antidote should be used, fomepizole or ethanol?. Netherlands Journal of Medicine. 2014;72(2):73–79.
13. El-Bakary A, others. Ranitidine as an alcohol dehydrogenase inhibitor in acute methanol toxicity in rats. Human and Experimental Toxicology. 2010;29(2):93–101.
14. Alnefaie SA, others. Methanol intoxication in the central region of Saudi Arabia: Five case studies. Saudi Pharmaceutical Journal. 2024;32(3):102018.
15. Alqurashi GI, others. Case Reports Study on Methanol Poisoning in King Abdul Aziz Specialist Hospital. Journal of Clinical Medicine. 2023;12(13):4282.
16. Alerta Epidemiológico: Envenenamento por Metanol nas Américas. 2025.
17. Mégarbane B. Treatment of patients with ethylene glycol or methanol poisoning: focus on fomepizole. Open Access Emergency Medicine. 2010;2:67–75.
18. Hantson P, others. Methanol poisoning and organ transplantation. Transplantation. 1999;68(1):165–167.
19. European Association of Poisons Centres, Clinical Toxicologists. Position paper on the treatment of methanol poisoning. Clinical Toxicology. 2023;61(1):1–13.
20. Zakharov S, others. Intermittent hemodialysis is superior to CVVHD/HDF to eliminate methanol and formate. Kidney International. 2014;86(1):199–207.
21. AOAC International. Official Methods of Analysis, Method 942.06: Alcohol by Volume in Distilled Liquors. AOAC International. 2023.
22. ANP. 2022.
23. ABNT. 2012.
24. van den Broek J, others. Screening Methanol Poisoning with a Portable Breath Detector. Analytical Chemistry. 2021;93(2):1170–1178.
25. OIML. International Alcoholometric Tables. OIML R 22-1. Paris: OIML. 1975.
26. Osborne NS, McKelvy EC, Bearce HW. Density and Thermal Expansion of Ethyl Alcohol and of Its Mixtures with Water. Bulletin of the Bureau of Standards. 1913;9:327–474.
27. Revista AdNormas. 2018. [Link](https://revistaadnormas.com.br/2018/11/06/a-determinacao-da-massa-especifica-no-etanol-combustivel)
28. Lachenmeier DW, others. Application of tailored reference materials and metrologically consistent methods for the analysis of alcoholic beverages. Journal of Consumer Protection and Food Safety. 2021;16:215–228.
29. Carneiro HSP, Medeiros AR, Oliveira FCC, Aguiar GM, Rubim JC, Suarez PAZ. Determination of Ethanol Fuel Adulteration by Methanol Using Partial Least-Squares Models Based on Fourier Transform Techniques. Energy \& Fuels. 2008;22(4):2767–2770. doi:[10.1021/ef8000218](https://doi.org/10.1021/ef8000218)
30. Silva AC, Pontes LFBL, Pimentel MF, Pontes MJC. Detection of adulteration in hydrated ethyl alcohol fuel using infrared spectroscopy and supervised pattern recognition methods. Talanta. 2012;93:129–134. doi:[10.1016/j.talanta.2012.01.060](https://doi.org/10.1016/j.talanta.2012.01.060)
31. Lopes Jesus AJ, others. Theoretical Prediction of Thermal Diffusion in Water–Methanol, Water–Ethanol, and Water–Isopropanol Mixtures. Journal of Physical Chemistry B. 2006;110(46):23180–23188.
32. Osborne S. Determination of Density, Alcohol Content, and Extract in Alcoholic Beverages. Journal of AOAC. 1987;70(6):1006–1009.
33. Dizechi M, Marschall E. Viscosity of Some Binary and Ternary Liquid Mixtures. Journal of Chemical and Engineering Data. 1982;27(3):358–363.
34. Guevara-Carrion G, Vrabec J, Hasse H. Prediction of self-diffusion coefficient and shear viscosity of water and its binary mixtures with methanol and ethanol by molecular simulation. Journal of Chemical Physics. 2011;134(7):074508.
35. Grunberg L, Nissan AH. Mixture Law for Viscosity. Nature. 1949;164(4175):799–800.
36. Redlich O, Kister AT. Algebraic Representation of Thermodynamic Properties and the Classification of Solutions. Industrial and Engineering Chemistry. 1948;40(2):345–348.
37. Wang X, others. Excess Properties, Computational Chemistry, and Spectral Analysis of [Diethanolamine + Alcohols] Ion-Like Liquids. Journal of Chemical and Engineering Data. 2023;68(10):2510–2524.
38. Domanska U, Laskowska M. Temperature and Composition Dependence of the Density and Viscosity of Binary Mixtures of \1-Butyl-3-methylimidazolium Thiocyanate + 1-Alcohols\. Journal of Chemical and Engineering Data. 2009;54(9):2113–2119.
39. Haghbakhsh R, Duarte ARC, Raeissi S. Viscosity Investigations on the Binary Systems of (1 ChCl:2 Ethylene Glycol) DES and Methanol or Ethanol. Molecules. 2021;26(18):5513.
40. JCGM. Evaluation of measurement data –- Guide to the expression of uncertainty in measurement (GUM). JCGM 100:2008. 2008.
41. JCGM. Supplement 1 to the GUM: Propagation of distributions using a Monte Carlo method. JCGM 101:2008. 2008.
42. Cox MG, Siebert BRL. The use of a Monte Carlo method for evaluating uncertainty and expanded uncertainty. Metrologia. 2006;43(4):S178–S188.
43. Possolo A. Copulas for uncertainty analysis. Metrologia. 2010;47(3):262–271.
44. Liu F, Liu Y, Wu S. Evaluating methods of calculating measurement uncertainty. Accreditation and Quality Assurance. 2011;16(1):1–7.
45. Paasma R, others. Risk factors related to poor outcome after methanol poisoning. Clinical Toxicology. 2012;50(9):823–831.
46. Vale A. Methanol. Medicine. 2007;35(12):633–634.
47. Barceloux DG, others. American Academy of Clinical Toxicology practice guidelines on the treatment of methanol poisoning. Journal of Toxicology: Clinical Toxicology. 2002;40(4):415–446.
Quer testar a triagem de metanol agora?
Acessar o AlcoLab